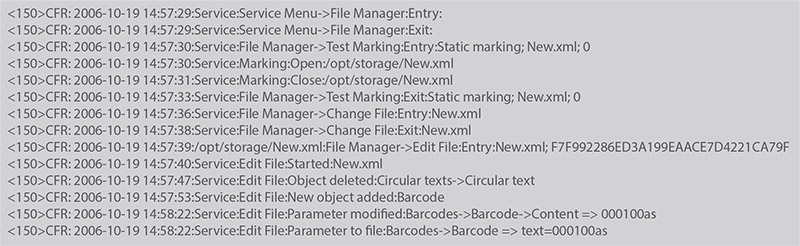
Jednoducho ide o uchovanie dát a dokumentov v podobe elektronického záznamu, kedy je generovaný väčšinou textový dokument, obsahujúci záznam o prihlásení do systému, prevedené zmeny a následnú prevádzku zariadení.
Ide o taký log-file, ktorý má validitu vďaka zaheslovanému prístupu do systému.
Laser systém a FDA 21 CFR Part 11
Laserové systémy Solaris ponúkajú tieto voľby pre splnenie uvedených požiadaviek:
- Použitie ovládania laseru v niekoľkých úrovniach hesiel a prístupov k ovládaniu
- Logging, alebo záznam všetkých aktivít užívateľa s časovým údajom a užívateľskými zmenami („audit trail“)
- Logging, alebo záznam všetkých systémových stavov s časovými údajmi. Napríklad chybové hlásenie.
- Rozšírený komunikačný protokol pre integráciu do zákazníckej siete s centralizovanou správou a užívateľskými dátami (ERP systémy a napríklad SAP R3)
- Dátová bezpečnosť via Windows WP Professional, NTFS súborový systém a neprerušenie napájanie vďaka UPS
História FDA 21 CFR Part 11
Už roku 1991 sa podniky, ktorých výrobný program v USA podliehal štátnemu (federálnemu ) dozoru, začali pýtať na FDA Amerického úradu pre potraviny a liečivá (U.S. Food and Drug Administration- FDA), ako a kedy by mohli namiesto dokumentácie vedenej na papieri začať používať elektronické záznamy a tzv. elektronický podpis.
Nasledovalo vydanie smernice FDA v auguste roku 1997, skrátene označovanú ako 21 CFR Part 11 (FDA: Part 11 of Title 21 of the Code of Federal Regulations: Electronic records; electronic signatures). Smernica CFR 21 Part 11 stanovuje, že výrobné spoločnosti, ako z oboru farmácie, tak aj potravinárstva, môžu používať validitu elektronických záznamov a podpisy. Pre tých, ktorí pri výrobe alebo distribúcii výrobkov podliehajú dozoru zo strany FDA (tzv. regulované produkty) a používajú počítačové systémy, je použitie elektronických záznamov a podpisov doslova povinné. Smernica 21 CFR Part 11 stanovuje procedúry a technické požiadavky, ktoré sú podmienkou použitia počítačových systémov založené na elektronickom uchovaní dať a využívajúcich elektronický podpis. Určuje spôsoby validácie počítačového systému, autentizácia užívateľa, prístupu k systému a jeho zabezpečenie, použitie časových značiek, uchovanie podkladov pre audit, príjmu záznamov a stanovuje, čo je treba predovšetkým brať v úvahu pri identifikácii požadovaného záznamu. Smernica 21 CFR Part 11 je dôležitá preto, že FDA, a spolu s ním pravdepodobne tiež ďalšie dohliadajúce úrady auditu a v nepodelenej rade aj mnohí vedúci pracovníci v podnikoch, budú uchovávať dáta v elektronickej forme záznamu. Smernica stanovuje, že elektronický vytvorené výrobné dáta vyžadujú inšpekciu auditu a elektronickú archiváciu.
Jednoduchosť implementácie
Vďaka pripravenosti zariadení na uvedenú normu zhody s 21 CFR Part 11 ide o veľmi lacnú, finančne a administratívne nenáročnú implementáciu, ktorá významne neovplyvní hospodárenie firmy. Je tu zabezpečená prenositeľnosť dát a ich jednoduchá požadovaná archivácia.
Budúcnosť a 21 CFR Part 11
S rastom zložitosti systémov pre automatizáciu procesov používaných vo farmaceutickej a potravinárskej výrobe a súčasne s rastúcou angažovanosťou štátnych dohliadajúcich inštitúcii, ako je napr. FDA v USA, v oblasti validácie počítačových riadiacich systémov, je zjavná potreba v praxi používaného systému, ktorý umožní tieto systémy špecifikovať, konštruovať a validovať. Takýmto systémom je FDA 21 CFR Part 11.
Norma u nás
U nás je dozerajúcim orgánom v oblasti farmácie Štátny ústav pre kontrolu liečiv (SÚKL). Ďalej SÚKL konštatuje, že pokiaľ by u nás mal výrobca elektronicky vedené záznamy o prerušení šarží (tj. vrátane elektronických podpisov) a jeho počítačový systém by bol validovaný, pravdepodobne by nenarazil na problémy, a to tiež vďaka tomu, že rámci EU zatiaľ nebol vydaný žiadny pokyn, ktorý by toto detailne upravoval. Súčasná globálna povaha výroby aj spotreby, nie tak zriedka prichádzajú premeny osvedčených nadnárodných, firemných apod. štandardov vo všeobecne medzinárodne prijímanej de facto štandardy a v neposlednej rade aj skúsenosť, že niektorý výrobcovia a dodávatelia už spomínajú smernicu 21 CFR Part 11 v súvislosti s vlastnosťami ich ponúkaných produktov, nebráni produkciu v rámci EU. Smernica 21 CFR Part 11 v túto chvíľu predstavuje metódu valorizácie počítačových riadiacich systémov v automatizovanej priemyselnej výrobe, v princípe overenú, silno podporovanú a všeobecne dobre prijateľnú.